In de medische gezondheidszorg is er nog weinig aandacht voor vroegsignalering van insulineresistentie, dit terwijl mogelijk een groot deel van uw patiënten hiermee te maken heeft (naar schatting heeft zo’n 90% van de mensen in de Westerse wereld insulineresistentie). Doordat er weinig aandacht is voor vroegsignalering, wordt het vaak te laat herkend en erkend. Daarnaast bestaat het idee dat insulineresistentie vooral diabetes type 2 veroorzaakt. Dit terwijl er veel andere welvaartsziekten veroorzaakt worden door insulineresistentie. Denk hierbij aan onder meer overgewicht, hart- en vaatziekten en leververvetting.
In dit artikel geef ik u kort uitleg over wat insulineresistentie is en waarom dit vaak over het hoofd gezien wordt. Ook beschrijf ik bij welke patiënten er extra aandacht moet zijn voor (het risico op) insulineresistentie en breng ik verschillende ziekten die veroorzaakt of sterk beïnvloed worden door insulineresistentie in kaart. Tot slot doe ik een oproep en geef ik een advies met betrekking tot het ‘behandelen’ van insulineresistentie.
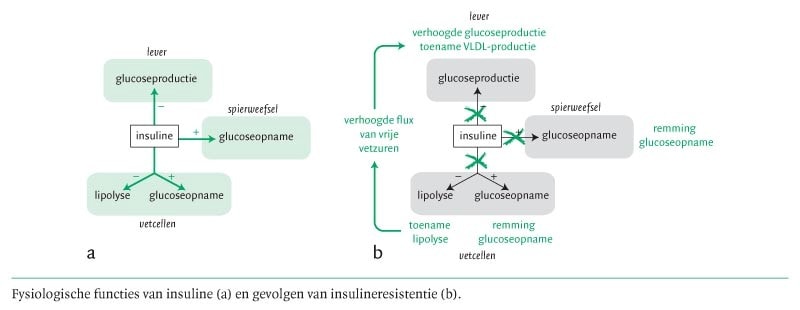
Insuline en insulineresistentie
In bovenstaande afbeelding is te zien dat insuline een belangrijke rol speelt binnen onder meer de glucoseopname in de doelorganen. Wanneer er sprake is van insulineresistentie nemen de cellen in de doelorganen glucose minder goed op. Normaal gesproken zou de glucosewaarde daardoor stijgen. Het lijf streeft echter naar normale glucosewaarden. Om deze normale glucosewaarden te kunnen handhaven heeft het een ‘slim’ compensatiemechanisme ontwikkeld: het reageert op insulineresistentie door nóg meer insuline te produceren (hyperinsulinemie). Hierdoor is het lichaam vaak toch nog lange tijd in staat om de glucosewaarden binnen de streefwaarden te houden. Dit is een stadium dat vaak niet herkend wordt, maar al wel schade toebrengt (Ref 1).
Een van de oorzaken van het niet herkennen van de hyperinsulinemie is dat insuline niet standaard wordt onderzocht binnen een bloedonderzoek (vaak wordt enkel nuchter glucose en HbA1c geprikt). Het kan zo zijn dat uw patiënt normale bloedsuikerwaarden en een normaal HbA1c heeft, maar toch te maken heeft met insulineresistentie. Zolang het bovenstaande compensatiemechanisme (waarbij hyperinsulinemie optreedt) voldoende werkt, zal insulineresistentie niet zichtbaar zijn in deze bloedonderzoeken. Daarvoor is minimaal een HOMA-IR nodig. Pas op het moment dat het compensatiemechanisme niet meer voldoende werkt, gaan vaak alarmbellen rinkelen. Dit is het moment dat uw patiënt hogere bloedsuikers krijgt: (pre-)diabetes is geboren (Ref 1).
HOMA-IR berekenen? Dat kan op deze website
U heeft hiervoor enkel een nuchter insuline en een nuchtere bloedglucose nodig
Insulineresistentie herkennen
Ondanks dat in een bloedonderzoek insulineresistentie pas zichtbaar is na het prikken van een HOMA-IR, zijn er wel lichamelijke kenmerken waaruit het vermoeden kan ontstaan dat iemand insulineresistent is. De praktijk wijst uit dat wanneer uw patiënt te maken heeft met één of meerdere van deze symptomen, de kans groot is dat uw patiënt te maken heeft met insulineresistentie.
Welke (uiterlijke) symptomen passen bij insulineresistentie:
- Overgewicht, met name in de buikregio;
- Een verstoord gevoel van honger en verzadiging;
- Vermoeidheid na het eten van koolhydraatrijke voeding;
- Donkere huidverkleuring (oksels, liezen, bilnaad, onder de borsten, rond de navel);
- Een hoge bloeddruk.
Sommige mensen hebben een groter risico op het ontwikkelen van (complicaties bij) insulineresistentie. Bij hen is extra aandacht geboden. Het gaat om:
- Mensen van Surinaams-Hindoestaanse, Turkse of Marokkaanse afkomst;
- Vrouwen die zwangerschapsdiabetes hebben gehad;
- Vrouwen die een baby van meer dan 9 pond hebben gebaard;
- Mensen die medicatie als steroïden, antipsychotica en HIV remmers gebruiken.
VERBAND TUSSEN VERSCHILLENDE AANDOENINGEN EN INSULINERESISTENTIE
OVERGEWICHT EN INSULINERESISTENTIE
HART- EN VAATZIEKTEN EN INSULINERESISTENTIE
LEVERVERVETTING (NAFLD en NASH) EN INSULINERESISTENTIE
NIERFALEN EN INSULINERESISTENTIE
ALZHEIMER EN INSULINERESISTENTIE
PCOS EN INSULINERESISTENTIE
KANKER EN INSULINERESISTENTIE
CONCLUSIE, OPROEP EN BEHANDELING INSULINERESISTENTIE
Obesitas en insulineresistentie
Obesitas wordt in veel gevallen veroorzaakt door insulineresistentie. Wat we vaak tegenkomen in de medische wereld is het idee dat mensen met obesitas simpelweg te veel eten en te weinig bewegen. Dit blijkt in de meeste gevallen niet de oorzaak van obesitas. Obesitas wordt veroorzaakt door een hormoondisbalans, met in bijna alle gevallen insuline als hoofdrolspeler. In de praktijk zien we erg vaak dat mensen onder begeleiding meestal wel af kunnen vallen, maar dat dit gewichtsverlies tijdelijk is en dat volgende afvalpogingen steeds moeilijker worden. Gesteld kan worden dat zolang insulineresistentie niet wordt aangepakt, de daadwerkelijke oorzaak van obesitas niet wordt aangepakt en gewichtsverlies moeizaam verloopt of niet blijvend is.
Insuline is een hormoon dat ervoor zorgt dat het lichaam vet gaat opslaan, het zorgt er voor dat een teveel aan koolhydraten (bloedglucose) direct wordt opgeslagen in de vetreserves. In 2001 werd in een onderzoek (Ref 2) al aangegeven dat koolhydraatrijk eten lipogenese stimuleert doordat deze koolhydraten insulineafgifte stimuleren en glucagonafgifte remmen. In dit onderzoek wordt aangegeven dat insuline het meest invloedrijk is als het gaat om vetopslag. Een ander onderzoek (Ref 3) geeft aan dat insulineresistentie vooral plaatsvindt in weefsels/doelorganen, maar dat het lipogene effect van insuline blijft bestaan. Hierdoor bereikt glucose minder makkelijk de weefsels/doelorganen, maar wordt dit onder invloed van insuline steeds makkelijker als vet opgeslagen in de vetcellen. Hieruit kan worden opgemaakt dat hoe insulineresistenter uw patiënt is, hoe makkelijker het lichaam van uw patiënt vet opslaat in de vetcellen.
Dr. Lustig voegt hier in een lezing (Ref 4) aan toe: “Hoe meer insuline je aanmaakt, hoe meer vet je aanmaakt.” Ook geeft hij in deze lezing aan, dat insuline zorgt voor leptineresistentie. Leptine zorgt in normale situaties voor het gevoel van verzadiging. Onder invloed van insuline wordt de werking van leptine geblokkeerd. Daardoor zijn mensen met insulineresistentie geneigd sneller te veel te eten, wat leidt tot meer vetopslag. Hij benoemt dat het noodzakelijk is om insulineniveaus te verlagen middels aanpassingen in dieet, als het gaat om het voorkomen en behandelen van obesitas. Templeman, Skovsø, Page, Lim, & Johnson (Ref 5) bevestigen dit en geven aan dat dieetwijzigingen die ervoor zorgen dat insulineniveaus dalen, de meest effectieve oplossing zijn in het voorkomen en genezen van obesitas.
Wat kunnen u en uw patiënt verwachten van een koolhydraatarme/keto aanpak?
Wanneer uw patiënt koolhydraatarm/keto gaat eten, verlagen insulinelevels direct. Hierdoor wordt het steeds makkelijker om uit de vetopslagzone te komen en in de vetverbrandingzone te komen. Hierdoor wordt het voor uw patiënt weer mogelijk om blijvend gewicht te verliezen.
Hart- en vaatziekten en insulineresistentie
Hypertensie
Al in 1987 werd benoemd in een onderzoek van Ferrannini et al. (Ref 6) dat hypertensie een symptoom is van insulineresistentie. Ook blijkt dat 50 procent van de mensen met hypertensie glucoseintolerant is (Ref 7). Een recent onderzoek van Tsimihodimos, Gonzalez-Villalpando, Meigs, & Ferrannini (Ref 8) geeft zelfs aan, dat hypertensie een vroege voorspeller is van het ontwikkelen van diabetes type 2 en dat de belangrijkste oorzaak van hypertensie wel eens insulineresistentie zou kunnen zijn. De oorzaken die zij hiervoor geven zijn: proliferatie van vasculaire gladde spiercellen en verhoogde vasculaire stijfheid, direct en indirect schaden van vasodilatatie, verhoging van oxidatieve stress en het veroorzaken van ontstekingen in de vaatwand. De gevolgen hiervan zijn verminderde autoregulatie van de vaattonus, verhoogde vaatweerstand en bloeddrukverhoging. Ook zou het antidiuretische effect van insuline ervoor zorgen dat er natrium wordt vastgehouden in de nieren, wat ook kan leiden tot hypertensie. Petrie, Guzik & Touyz (Ref 9) geven de volgende verstoringen als oorzaak van hypertensie door insulineresistentie: upregulatie van het RAAS, oxidatieve stress en ontsteking en activering van het immuunsysteem. Deze komen overeen met de oorzaken die het eerdere onderzoek van Tsimihodimos, et al. (Ref 8) beschrijft.
Wat kunnen u en uw patiënt verwachten van een koolhydraatarme/keto aanpak?
In de praktijk blijkt dat een hoge bloeddruk in bijna alle gevallen aangepakt kan worden door koolhydraatarm/keto te gaan eten. We zien binnen enkele maanden verbeteringen in de systolische en diastolische bloeddruk. Aanpassen van medicatie is vaak al snel nodig om hypotensie te voorkomen. Wanneer u bij uw patiënt na 6 maanden nog geen verbetering heeft waargenomen, is de kans groot dat de oorsprong van de problematiek geen insulineresistentie is. Nader onderzoek naar de oorzaak van de problematiek is dan noodzakelijk.
Verhoogd cholesterol
Dyslipidemie wordt als belangrijke oorzaak van hart- en vaatziekten gezien. Het gaat hierbij vooral om verhoogde triglyceriden en sdLDL. Uit recent onderzoek (Ref 10) blijkt dat insulineresistentie niet alleen effect heeft op het glucosemetabolisme, maar ook op het vetmetabolisme. Het kan leiden tot dyslipidemie, waarbij er onder meer hogere triglyceriden, lagere HDL- en hogere sdLDL- gehalten worden waargenomen. Ook in de nieuwe NHG-standaard (Ref 11) wordt er niet direct en alleen gefocust op LDL, maar wordt er vooral gekeken naar de ratio en andere risicofactoren voor hart- en vaatziekten.
Wat kunnen u en uw patiënt verwachten van een koolhydraatarme/keto aanpak?
In de praktijk zien we dat cholesterolratio’s en de triglyceridenwaarde vrijwel direct verbeteren. Er kan een tijdelijke toename zijn van het LDL, maar dat wordt niet als schadelijk gezien. Naar verwachting normaliseert het LDL binnen 6 maanden en wordt hij vaak lager dan de startwaarde.
Meer over cholesterol en de koolhydraatarme/keto aanpak? Ik schreef dit artikel voor zorgprofessionals.
Artherosclerose
Insulineresistentie speelt een rol binnen het ontstaan van artherosclecrose. Het onderzoek van Won et al. (Ref 12) beschrijft dit aan de hand van de TyG-index; een screeningsmethode voor insulineresistentie. Uit hun onderzoek blijkt dat mensen met een hogere mate van insulineresistentie meer risico hebben op het ontwikkelen van artherosclerose. Het onderzoek van Ormazabal et al. (Ref 10) beschrijft dat insulineresistentie artherosclerose kan veroorzaken doordat het, samen met beschadiging van de vaatwand, dyslipidemie veroorzaakt.
Wat kunnen u en uw patiënt verwachten van een koolhydraatarme/keto aanpak?
Door koolhydraatarm/keto te gaan eten ontstaan er minder vaatwandbeschadigingen. Het blijkt dat schommelende bloedsuikers, onder invloed van insulineresistentie deze vaatwandbeschadigingen veroorzaken. Cholesterol wil deze vaatwandbeschadigingen repareren, waardoor er artherosclerose ontstaat. Het risico op ontwikkelen van artherosclerose is, wanneer iemand koolhydraatarm/keto eet, sterk vermindert.
Cardiomyopathie of hartfalen
Bekend is dat mensen met diabetes een grotere kans hebben op het ontwikkelen van cardiomyopathie of hartfalen. Uit recent onderzoek (Ref 13) blijkt dat iemand die geen diabetes heeft, maar wel insulineresistent is, ook een verhoogd risico heeft op het ontwikkelen van cardiomyopathie. In dit onderzoek wordt beschreven dat hyperinsulinemie en hyperglycemie beide onafhankelijke risicofactoren zijn in het ontwikkelen van cardiomyopathie. Hieraan ten grondslag liggen volgens de onderzoekers onder meer de volgende gevolgen van insulineresistentie: cardiale insulineresistentie, glucotoxiciteit, mitochondriale disfunctie, oxidatieve stress, verstoringen in het RAAS-systeem, verminderde mitofagie en autofagie en coronaire microvasculaire disfunctie.
Ook het onderzoek van Varma, Koutsifeli, Benson, Mellor, & Delbridge (Ref 14) beschrijft dat insulineresistentie een oorzaak is van cardiomyopathie. Zij beschrijven het volgende: “Verminderde glucose-opname als gevolg van insulineresistentie en verminderde expressie van glucosetransporters wordt geassocieerd met een verschuiving naar een verhoogde afhankelijkheid van vetzuuroxidatie en verminderde cardiale efficiëntie in diabetische harten.” Daarnaast geven zij aan dat metabole dysregulatie, waar insulineresistentie onderdeel van is, in verband wordt gebracht met oxidatieve stress, verminderde mitochondriale functie en autofagiestoornissen. Dit kan leiden tot celdood en fibrosevorming, met hartfalen tot gevolg.
Wat kunnen u en uw patiënt verwachten van een koolhydraatarme/keto aanpak?
Wanneer uw patiënt koolhydraatarm/keto gaat eten, is de kans groot dat de cellen beter gaan reageren op glucose. Daarnaast is er voldoende aanwezigheid van effectief bruikbare energie in de vorm van vetzuren en ketonen. De kans is groot dat het risico op cardiomyopathie en hartfalen vermindert en dat (een gedeelte van de) reeds ontstane schade teruggedraaid kan worden.
Non-alcoholische leververvetting en insulineresistentie
In het artikel van Finck (Ref 15) wordt beschreven dat er een sterke link is tussen non-alcoholische leververvetting (NAFLD) en insulineresistentie. Hierbij wordt gekeken naar NAFLD in een breed spectrum van aandoeningen die variëren van eenvoudige steatose (NAFL) tot steatose met inflammatoire laesies (NASH). De progressie van NAFL naar NASH blijkt onder andere veroorzaakt te worden door insulineresistentie.
De verwachting is dat de dyslipidemie, veroorzaakt door insulineresistentie, zorgt voor vervetting van de lever. Ook zou de stofwisseling van hepatocyten verstoord raken door insulineresistentie: er is sprake van verhoogde lipogenese in de levercellen en een verhoogd vetzuurtransport richting de levercellen. Daarnaast is de lever minder goed in staat opgeslagen vetten af te breken door een verstoring in autofagie en een opstapeling van kapotte mitochondria. Hierdoor ontstaat in eerste instantie NAFL en kan uiteindelijk NASH ontstaan. Beschreven wordt dat het verbeteren van insulinesensitiviteit de meest effectieve manier is om NAFLD en NASH te behandelen (Ref 15, Ref 16).
Wat kunnen u en uw patiënt verwachten van een koolhydraatarme/keto aanpak?
In de pratijk blijkt dat een koolhydraatarme/keto aanpak effectief is als het gaat om omkeren van NAFLD. Leverwaarden normaliseren binnen enkele maanden (afhankelijk van de ernst van de leververvetting). Naar verwachting kan (een gedeelte van de) reeds ontstane schade worden teruggedraaid.
Nierfalen en insulineresistentie
Nierfalen komt vaak voor bij mensen die (vaak in ernstige mate) insulineresistent zijn. De invloed die insulineresistentie hierin speelt wordt beschreven door een artikel van Spoto, Pisano, & Zoccali (Ref 17). Zij geven aan dat hyperinsulinemie onder meer activering van het sympathisch zenuwstelsel, natriumretentie, downregulatie van het natriuretische peptidesysteem, toename van albuminesecretie en het ontstaan van nierfibrose veroorzaakt. Ook de invloed die insulineresistentie op het cardiovasculaire systeem heeft draagt bij aan het ontwikkelen van nierfalen.
Een ander onderzoek (Ref 18) vult aan dat insulineresistentie zorgt voor oxidatieve stress en ontstekingsreacties die een negatieve invloed hebben op de nierfunctie, doordat zij kunnen zorgen voor endotheliale disfunctie, activering van het RAAS en disbalans van adipokines. Ook de schade die insulineresistentie aanbrengt in de mitochondriale werking kan progressie van nierschade in de hand werken.
Wat kunnen u en uw patiënt verwachten van een koolhydraatarme/keto aanpak?
In de praktijk blijkt dat nierfalen, waarbij insulineresistentie ten grondslag ligt (dus niet met andere onderliggende oorzaak), (gedeeltelijk) kan worden teruggedraaid wanneer uw patiënt koolhydraatarm/keto gaat eten. Nierfuncties worden vaak binnen enkele maanden sterk verbeterd.
Alzheimer en insulineresistentie
Inmiddels wordt Alzheimer steeds vaker diabetes type 3 genoemd. En niet voor niks: er zijn steeds meer bewijzen dat Alzheimer veroorzaakt wordt door insulineresistentie. Het blijkt dat gebieden in het brein die gevoelig zijn voor het ontstaan van Alzheimer erg te lijden hebben onder insulineresistentie: door de insulineresistentie hebben zij niet meer voldoende toegang tot glucose. Dit ontstaat al bij milde insulineresistentie, die niet altijd opgemerkt wordt (Ref 19).
Daarnaast zou diabetes type 2, veroorzaakt door insulineresistentie, invloed hebben op het functioneren van pericyten en de bloedbreinbarrière. Dit zou resulteren in een toename van eiwitstapeling in het brein, wat dementie zou kunnen veroorzaken. Het lymfesysteem is ook negatief beïnvloed en kan eiwitten minder goed opruimen, wat bijdraagt aan verergering van klachten. Dit draagt tevens bij aan het ontstaan van ontstekingsreacties in het brein (Ref 20), (Ref 21).
Naast de directe invloed van insulineresistentie op het brein, heeft insulineresistentie ook invloed op de vaatconditie. Vaten in het brein raken beschadigd door hoge bloedsuikers en hoge insulinelevels. Hierdoor treedt vasculaire schade en verminderde bloedstroom in de hersenen op. Het gevolg hiervan is dat er onvoldoende zuurstof, voedingsstoffen en glucose in het brein terecht komen. Door onvoldoende zuurstof ontstaat er daarnaast oxidatieve stress in het brein, waardoor er ontstekingsreacties ontstaan, die ook bijdragen aan het ontstaan van Alzheimer (Ref 20).
Wat kunnen u en uw patiënt verwachten van een koolhydraatarme/keto aanpak?
Door koolhydraatarm/keto te gaan eten kan het risico op ontstaan van Alzheimer sterk worden teruggedrongen. Daarnaast bestaat de kans dat progressie van de ziekte wordt vertraagd of tot stilstand wordt gebracht. Ook kan het zijn dat uw patiënt verbetering van cognitieve functies waarneemt wanneer hij/zij koolhydraatarm/keto gaat eten.
PCOS en insulineresistentie
Dr. Fung (Ref 22) geeft aan dat nagenoeg alle vrouwen met overgewicht en PCOS insulineresistent zijn en dat minstens 75 procent van de vrouwen met een normaal gewicht en PCOS insulineresistent is. In diverse onderzoeken (Ref 23, Ref 24, Ref 25, Ref 26) wordt aangegeven dat er bij PCOS onder meer sprake is van glucose-intolerantie in de eierstokken. In reactie hierop gaan de eierstokken extra androgenen produceren. Dit leidt tot het sterke vermoeden dat hyperandrogenisme samenhangt met een verstoring in de insulinehuishouding (hyperinsulinemie). Ook kenmerkend is dat een derde van de jongeren met PCOS en ruim de helft van volwassenen met PCOS kenmerken heeft van het metaboolsyndroom (een verzameling van klachten die, uiteengezet in dit artikel, ook gevolgen zijn van insulineresistentie) en/of diabetes type 2.
Wat kunnen u en uw patiënt verwachten van een koolhydraatarme/keto aanpak?
In de praktijk blijkt dat de koolhydraatarme/keto aanpak zorgt voor een verbetering in hormoonbalans bij vrouwen met PCOS. Regelmatig horen wij dat vrouwen met PCOS nadat zij koolhydraatarm/keto zijn gaan eten bijvoorbeeld meer regelmatige cycli krijgen en in staat zijn om op een natuurlijke manier zwanger te worden (zonder hormoontherapie). Daarnaast lopen zij minder risico op andere metabole ziekten (bijv dyslipidemie en diabetes type 2) wanneer zij koolhydraatarm/keto gaan eten.
Kanker en insulineresistentie
Het hebben van diabetes type 2, veroorzaakt door insulineresistentie, vergroot de kans op het ontwikkelen van diverse kankersoorten, onder meer: darm-, lever-, alvleesklier-, borst-, baarmoeder-, en blaaskanker. Uit een grote cohortstudie (Ref 27) blijkt dat mensen die nog geen diabetes type 2 hebben, maar wel insulineresistent zijn, ook een vergroot risico hebben op het ontwikkelen van diverse vormen van kanker.
In een artikel van Kim & Dang (Ref 28) wordt genoemd dat dit mogelijk wordt veroorzaakt door het Warburg-effect: door hyperglycemie is de tumor in staat zich te voeden en wordt groei van de tumor vergemakkelijkt.
Een andere studie (Ref 29) wijt de vergrote kans op het ontstaan van bovenstaande tumoren aan het groeibevorderende effect van insuline. In verschillende studies wordt dit idee ondersteund. Metformine zou het ontstaan en de groei van deze tumoren verminderen, terwijl exogene insuline de groei zou bevorderen (Ref 30, Ref 31, Ref 32, Ref 33, Ref 34, Ref 35).
Wat kunnen u en uw patiënt verwachten van een koolhydraatarme/keto aanpak?
Door koolhydraatarm/keto te gaan eten vermindert uw patiënt het risico op het ontwikkelen van bovengenoemde kankersoorten. Daarnaast bestaat er de kans dat al aanwezige maligniteiten worden teruggedrongen. Koolhydraatarm/keto eten zou een reguliere behandeling kunnen ondersteunen.
CONCLUSIE EN OPROEP: Insulineresistentie voorkomen en behandelen!
Zoals u heeft kunnen lezen, bestaat er een sterk verband tussen insulineresistentie en verschillende aandoeningen. Om deze aandoeningen effectief te behandeling, is het dus van belang om ervoor te zorgen dat insulineniveaus in het bloed dalen. Dit kan zowel preventief als curatief, simpelweg door uw patiënt koolhydraatarm/keto te laten eten.
Mijn oproep aan u allen is dan ook als volgt: voorkom en behandel insulineresistentie om zo de bovenstaande gevolgen hiervan te beperken. De koolhydraatarme/keto aanpak is een effectieve non-medicamenteuze methode (Ref 36, Ref 37, Ref 38). Wanneer iemand start met deze aanpak dalen bloedsuikers en insulinespiegels direct. De gevolgen van insulineresistentie nemen daardoor vrijwel altijd direct af!
U kunt hiervoor de STARTGIDS koolhydraatarm/keto eten adviseren. Hierin staat alle benodigde informatie en een eenvoudig, effectief en toegankelijk weekmenu. U vindt de STARTGIDS hier.
VERDER LEZEN….
De enige échte behandeling van DM2
Cholesterol en de koolhydraatarme/keto aanpak

Lara Schalk is verpleegkundige bij TheNewFood. Lara combineert haar medische achtergrond met haar schat aan kennis over gezonde koolhydraatarme/keto voeding. Ze schrijft onder andere artikelen voor de site en adviseert en begeleidt mensen, ook één op één. Kijk hier voor de mogelijkheden.
Heb je nog vragen na het lezen van deze informatie? Stuur een bericht.
LITERATUURLIJST
- Ref 1: Het metabool syndroom: een cluster van vasculaire risicofactoren. (2009, 3 december). Geraadpleegd op 16 augustus 2019, van https://www.ntvg.nl/artikelen/het-metabool-syndroom-een-cluster-van-vasculaire-risicofactoren
- Ref 2: Kersten, S. (2001). Mechanisms of nutritional and hormonal regulation of lipogenesis. EMBO reports, 2(4), 282–286. https://doi.org/10.1093/embo-reports/kve071
- Ref 3: Erion, K. A., & Corkey, B. E. (2017). Hyperinsulinemia: a Cause of Obesity? Current Obesity Reports, 6(2), 178–186. https://doi.org/10.1007/s13679-017-0261-z
- Ref 4: Lustig, R. (2011, 3 november). The cause of obesity [YouTube]. Geraadpleegd op 23 augustus 2019, van https://www.youtube.com/watch?v=m8dWNbEscOw
- Ref 5: Templeman, N. M., Skovsø, S., Page, M. M., Lim, G. E., & Johnson, J. D. (2017). A causal role for hyperinsulinemia in obesity. Journal of Endocrinology, 232(3), R173–R183. https://doi.org/10.1530/JOE-16-0449
- Ref 6: Ferrannini, E., Buzzigoli, G., Bonadonna, R., Giorico, M. A., Oleggini, M., Graziadei, L., … Bevilacqua, S. (1987). Insulin Resistance in Essential Hypertension. New England Journal of Medicine, 317(6), 350–357. https://doi.org/10.1056/NEJM198708063170605
- Ref 7: Mitchell, B. D., Stern, M. P., Haffner, S. M., Hazuda, H. P., & Patterson, J. K. (1990). Risk factors for cardiovascular mortality in Mexican Americans and no-Hispanic Whites. American Journal of Epidemiology, 131(3), 423–433. https://doi.org/10.1093/oxfordjournals.aje.a115517
- Ref 8: Tsimihodimos, V., Gonzalez-Villalpando, C., Meigs, J. B., & Ferrannini, E. (2018). Hypertension and Diabetes Mellitus. Hypertension, 71(3), 422–428. https://doi.org/10.1161/HYPERTENSIONAHA.117.10546
- Ref 9: Petrie, J. R., Guzik, T. J., & Touyz, R. M. (2018). Diabetes, Hypertension, and Cardiovascular Disease: Clinical Insights and Vascular Mechanisms. Canadian Journal of Cardiology, 34(5), 575–584. https://doi.org/10.1016/j.cjca.2017.12.005
- Ref 10: Ormazabal, V., Nair, S., Elfeky, O., Aguayo, C., Salomon, C., & Zuñiga, F. A. (2018). Association between insulin resistance and the development of cardiovascular disease. Cardiovascular Diabetology, 17(1). https://doi.org/10.1186/s12933-018-0762-4
- Ref 11: Cardiovasculair risicomanagement (CVRM) | NHG. (z.d.). Geraadpleegd op 19 augustus 2019, van https://richtlijnen.nhg.org/standaarden/cardiovasculair-risicomanagement#volledige-tekst
- Ref 12: Won, K.-B., Kim, Y. S., Lee, B. K., Heo, R., Han, D., Lee, J. H., … Chang, H.-J. (2018). The relationship of insulin resistance estimated by triglyceride glucose index and coronary plaque characteristics. Medicine, 97(21), e10726. https://doi.org/10.1097/MD.0000000000010726
- Ref 13: Jia, G., Whaley-Connell, A., & Sowers, J. R. (2017). Diabetic cardiomyopathy: a hyperglycaemia- and insulin-resistance-induced heart disease. Diabetologia, 61(1), 21–28. https://doi.org/10.1007/s00125-017-4390-4
- Ref 14: Varma, U., Koutsifeli, P., Benson, V. L., Mellor, K. M., & Delbridge, L. M. D. (2018). Molecular mechanisms of cardiac pathology in diabetes – Experimental insights. Biochimica et Biophysica Acta (BBA) – Molecular Basis of Disease, 1864(5), 1949–1959. https://doi.org/10.1016/j.bbadis.2017.10.035
- Ref 15: Finck, B. N. (2018). Targeting Metabolism, Insulin Resistance, and Diabetes to Treat Nonalcoholic Steatohepatitis. Diabetes, 67(12), 2485–2493. https://doi.org/10.2337/dbi18-0024
- Ref 16: Lindenmeyer, C. C., & McCullough, A. J. (2018). The Natural History of Nonalcoholic Fatty Liver Disease—An Evolving View. Clinics in Liver Disease, 22(1), 11–21. https://doi.org/10.1016/j.cld.2017.08.003
- Ref 17: Spoto, B., Pisano, A., & Zoccali, C. (2016). Insulin resistance in chronic kidney disease: a systematic review. American Journal of Physiology-Renal Physiology, 311(6), F1087–F1108. https://doi.org/10.1152/ajprenal.00340.2016
- Ref 18: Zhang, X., & Lerman, L. O. (2017). The metabolic syndrome and chronic kidney disease. Translational Research, 183, 14–25. https://doi.org/10.1016/j.trsl.2016.12.004
- Ref 19: Willette, A. A., Bendlin, B. B., Starks, E. J., Birdsill, A. C., Johnson, S. C., Christian, B. T., … Asthana, S. (2015). Association of Insulin Resistance With Cerebral Glucose Uptake in Late Middle–Aged Adults at Risk for Alzheimer Disease. JAMA Neurology, 72(9), 1013. https://doi.org/10.1001/jamaneurol.2015.0613
- Ref 20: Tumminia, A., Vinciguerra, F., Parisi, M., & Frittitta, L. (2018). Type 2 Diabetes Mellitus and Alzheimer’s Disease: Role of Insulin Signalling and Therapeutic Implications. International Journal of Molecular Sciences, 19(11), 3306. https://doi.org/10.3390/ijms19113306
- Ref 21: Pruzin, J. J., Nelson, P. T., Abner, E. L., & Arvanitakis, Z. (2018). Review: Relationship of type 2 diabetes to human brain pathology. Neuropathology and Applied Neurobiology, 44(4), 347–362. https://pubmed.ncbi.nlm.nih.gov/29424027/
- Ref 22: Fung, J. (2018, 15 november). PCOS and Hyperinsulinemia part 2. Geraadpleegd op 23 augustus 2019, van https://medium.com/@drjasonfung/pcos-and-hyperinsulinemia-part-2-f8f56fc4f161
- Ref 23: Anagnostis, P., Tarlatzis, B. C., & Kauffman, R. P. (2018). Polycystic ovarian syndrome (PCOS): Long-term metabolic consequences. Metabolism, 86, 33–43. https://doi.org/10.1016/j.metabol.2017.09.016
- Ref 24: Rosenfield, R. L., & Ehrmann, D. A. (2016). The Pathogenesis of Polycystic Ovary Syndrome (PCOS): The Hypothesis of PCOS as Functional Ovarian Hyperandrogenism Revisited. Endocrine Reviews, 37(5), 467–520. https://doi.org/10.1210/er.2015-1104
- Ref 25: De Leo, V., Musacchio, M. C., Cappelli, V., Massaro, M. G., Morgante, G., & Petraglia, F. (2016). Genetic, hormonal and metabolic aspects of PCOS: an update. Reproductive Biology and Endocrinology, 14(1). https://doi.org/10.1186/s12958-016-0173-x
- Ref 26: Torchen, L. C. (2017). Cardiometabolic Risk in PCOS: More than a Reproductive Disorder. Current Diabetes Reports, 17(12). https://doi.org/10.1007/s11892-017-0956-2
- Ref 27: Stocks, T., Borena, W., Strohmaier, S., Bjorge, T., Manjer, J., Engeland, A., … Stattin, P. (2009). Cohort Profile: The Metabolic syndrome and Cancer project (Me-Can). International Journal of Epidemiology, 39(3), 660–667. https://doi.org/10.1093/ije/dyp186
- Ref 28: Kim, J., & Dang, C. V. (2006). Cancer’s Molecular Sweet Tooth and the Warburg Effect: Figure 1. Cancer Research, 66(18), 8927–8930. https://doi.org/10.1158/0008-5472.CAN-06-1501
- Ref 29: Boyd, D. B. (2003). Insulin and Cancer. Integrative Cancer Therapies, 2(4), 315–329. https://doi.org/10.1177/1534735403259152
- Ref 30: Baur, D. M., Klotsche, J., Hamnvik, O.-P. R., Sievers, C., Pieper, L., Wittchen, H.-U., … Mantzoros, C. S. (2011). Type 2 diabetes mellitus and medications for type 2 diabetes mellitus are associated with risk for and mortality from cancer in a German primary care cohort. Metabolism, 60(10), 1363–1371. https://doi.org/10.1016/j.metabol.2010.09.012
- Ref 31: Soranna, D., Scotti, L., Zambon, A., Bosetti, C., Grassi, G., Catapano, A., … Corrao, G. (2012). Cancer Risk Associated with Use of Metformin and Sulfonylurea in Type 2 Diabetes: A Meta-Analysis. The Oncologist, 17(6), 813–822. https://www.ncbi.nlm.nih.gov/books/NBK109982/
- Ref 32: Chang, C.-H., Lin, J.-W., Wu, L.-C., Lai, M.-S., & Chuang, L.-M. (2012). Oral Insulin Secretagogues, Insulin, and Cancer Risk in Type 2 Diabetes Mellitus. The Journal of Clinical Endocrinology & Metabolism, 97(7), E1170–E1175. https://doi.org/10.1210/jc.2012-1162
- Ref 33: Chang, C.-H., Lin, J.-W., Wu, L.-C., Lai, M.-S., Chuang, L.-M., & Arnold Chan, K. (2012). Association of thiazolidinediones with liver cancer and colorectal cancer in type 2 diabetes mellitus. Hepatology, 55(5), 1462–1472. https://aasldpubs.onlinelibrary.wiley.com/doi/full/10.1002/hep.25509
- Ref 34: Colmers, I. N., Bowker, S. L., Majumdar, S. R., & Johnson, J. A. (2012). Use of thiazolidinediones and the risk of bladder cancer among people with type 2 diabetes: a meta-analysis. Canadian Medical Association Journal, 184(12), E675–E683. https://doi.org/10.1503/cmaj.112102
- Ref 35: Yang, Y., Hennessy, S., & Lewis, J. D. (2004). Insulin therapy and colorectal cancer risk among type 2 diabetes mellitus patients. Gastroenterology, 127(4), 1044–1050. https://doi.org/10.1053/j.gastro.2004.07.011
- Ref 36: Giannarelli, R., Aragona, M., Coppelli, A., & Del Prato, S. (2003). Reducing insulin resistance with metformin: the evidence today. Diabetes & Metabolism, 29(4), 6S28-6S35. https://doi.org/10.1016/S1262-3636(03)72785-2
- Ref 37: Krebs, J. D., Bell, D., Hall, R., Parry-Strong, A., Docherty, P. D., Clarke, K., & Chase, J. G. (2013). Improvements in Glucose Metabolism and Insulin Sensitivity with a Low-Carbohydrate Diet in Obese Patients with Type 2 Diabetes. Journal of the American College of Nutrition, 32(1), 11–17. https://doi.org/10.1080/07315724.2013.767630
- Ref 38: Hallberg, S. J., McKenzie, A. L., Williams, P. T., Bhanpuri, N. H., Peters, A. L., Campbell, W. W., … Volek, J. S. (2018). Effectiveness and Safety of a Novel Care Model for the Management of Type 2 Diabetes at 1 Year: An Open-Label, Non-Randomized, Controlled Study. Diabetes Therapy, 9(2), 583–612. https://doi.org/10.1007/s13300-018-0373-9